Генетическое обследование эмбрионов (ПГД, ПГС)
Когда пара с бесплодием приходит к врачу ее интересует множество вопросов. В процессе беседы может прозвучать аббревиатура ПГД.
Что это такое, для чего используется, нужно ли это именно в конкретном случае и что это даст?
Рисунок 1 Хромосомы и гены. Хромосомы — это «упакованные гены». Каждая хромосома содержит огромное количество генов. Хромосом всего 46 (23 пары). Каждые ген «закодирован» определенной последовательностью нуклеиновых кислот
Преимплантационная генетическая диагностика (ПГД)
Преимплантационная генетическая диагностика — это метод, используемый для выявления генетических дефектов у эмбрионов, полученных с помощью экстракорпорального оплодотворения (ЭКО).
Преимплантационная генетическая диагностика (ПГД) используется в случаях, когда один или оба генетических родителей имеют известную генетическую аномалию. В этом случае изучается эмбрион с целью выявления этой родительской аномалии. В основном это так называемые моногенные заболевания. Т.е.
заболевание связано с одним геном, а не с несколькими. Одно из самых часто встречающихся моногенных заболевании — это муковисцидоз (нарушение функций органов дыхания), носителем является 2-5% населения.
Чтобы заболевание проявилось необходимо чтобы встретились два носителя, при этом вероятность, что ребенок будет носителем — 50%, вероятность рождения больного, как и здорового ребенка составит — 25%. Частота рождения детей с муковисцидозом в России 1:10000.
Рисунок 2 По данным ОАО «Институт Стволовых Клеток Человека» http://www.rahr.ru/d_pech_mat_konf/schevchenko.pdf
Преимплантационная генетическая диагностика как раз и позволяет диагностировать заболевание у эмбриона еще до того, как его перенесут в полость матки.
Проводить преимплантационную генетическую диагностику всем подряд нет смысла. Это оправдано только в случае если известно, что родители либо болеют, либо являются носителями моногенного заболевания.
Таким образом, потребность в преимплантационной генетической диагностике очень маленькая и проводится не у пар, страдающих бесплодием, а у пар, где есть носительство или наличие моногенного заболевания.
На консультации по бесплодию речь идет о преимплантационном генетическом скрининге (ПГС), а не о ПГД. Просто как-то традиционно сложилось что ПГС называют ПГД.
Преимплантационный генетический скрининг (ПГС)
Преимплантационный генетический скрининг (ПГС) выполняется в случаях, когда эмбрионы от родителей с предположительно нормальным кариотипом (набором хромосом) изучаются на наличие анеуплоидии, т.е. нарушений набора хромосом. Самая частая хромосомная аномалия — трисомия по 21 паре, проявляется она в виде синдрома Дауна.
Рисунок 3 Риск рождения ребенка с синдромом Дауна в зависимости от возраста матери. NEWBERGER D. Down Syndrome: Prenatal Risk Assessment and Diagnosis. Am Fam Physician. 2000 Aug 15;62(4):825-832.
| Характеристика | Трисомия 21 | Трисомия 18 | Трисомия 13 |
| Эпоним | Синдром Дауна | Синдром Эдварда | Синдром Патау |
| Частота возникновения | 1:800 | 1:8000 | 1:15000 |
Риск всех хромосомных аномалий растет при увеличении возраста женщины.
Поскольку только эмбрионы с отсутствием известной патологии переносят в полость матки, преимплантационная диагностика является альтернативой диагностическим процедурам, проводимым с той же целью, но уже во время беременности (амниоцентез или биопсия хориона). При получении неудовлетворительных результатов после проведения биопсии хориона или амниоцентеза приходится принимать нелегкое решение о прерывании беременности.
В настоящее время ПГД и ПГС — это единственные доступные способы предотвращения зачатия ребенка, страдающего генетическим заболеванием. Огромный плюс этих методик, это отсутствие дилеммы прерывания уже наступившей беременности. Вся информация получается еще до наступления беременности.
Показания к преимплантационному генетическому скринингу (ПГС).
В настоящее время не существует конкретного перечня показаний для преимплантационного генетического скрининга (ПГС).
Самые ранние потери беременности связаны преимущественно с анеуплоидиями. Поскольку после ПГС, в полость матки переносят только эмбрионы с нормальным кариотипом, риск выкидышей заметно снижается.
Как правило, проведения ПГС рекомендуется в следующих группах:
- Женщины старше 35 лет
- Пары с привычным невынашиванием беременности
- Пары с повторными неудачными ЭКО
- Наличие тяжелого мужского бесплодия
У пациентов этих групп высокий риск неудачи при ЭКО из-за высокой вероятности наличия анеуплоидных эмбрионов. ПГС уменьшает этот риск, т.к. в полость матки переносят только эмбрионы с нормальным кариотипом, имеющие более высокий шанс имплантации.
Возраст женщины.
Риск анеуплоидии у детей возрастает по мере увеличения возраста женщин. Способность яйцеклетки давать нормальный эмбрион с возрастом теряется. Особенно значимо риск начинает увеличиваться после 35 лет.
Рисунок 4 Зависимость между возрастом матери и долей эмбрионов с хромосомными аномалиями.
Проведение ПГС у женщин старше 35 лет, увеличивает шанс на успешное ЭКО и, более того, резко снижает вероятность выкидышей. Собственно, шансы эмбриона с нормальным кариотипом не зависят от возраста матери.
Привычное невынашивание.
Под привычным невынашиванием понимают два и более выкидыша. В 50-80 % случаев выкидышей обнаруживают хромосомные аномалии. При привычном невынашивании доля эмбрионов с анеуплоидией еще выше. Проведение ПГС позволяет снизить частоту выкидышей, особенно в группе пациентов, где есть подтверждение анеуплоидии при предшествующих неудачных беременностях.
Повторные неудачи в ЭКО.
Под повторными неудачами в ЭКО обычно понимают 3 или более неудачных попыток ЭКО с переносом 4 и более эмбрионов высокого качества.
Имеющиеся данные свидетельствуют о том, что эти пациенты имеет бОльшее количество эмбрионов с хромосомными аномалиями. Проведение ПГС может существенно увеличить вероятность успешного ЭКО.
Но несмотря на успехи в диагностике хромосомных аномалий эмбрионов, остаются и другие причины повторных неудач, и далеко не все их них известны науке.
Наличие тяжелого мужского бесплодия
У мужчин с нарушением сперматогенеза выше вероятность того, что эмбрионы будут иметь хромосомные отклонения. У мужчин с нормальными показателями спермограммы среди сперматозоидов 3-8 % имеют хромосомные аномалии.
В то же время, у мужчин с тяжелыми нарушениями сперматогенеза (маленькая концентрация, подвижность и низкое количество сперматозоидов с нормальным строением) наличие хромосомно аномальных сперматозоидов существенно увеличивается.
Использование ИКСИ позволило преодолеть тяжелое мужское бесплодие и увеличило актуальность проведения ПГС у этих пар.
При мужском бесплодии чаще обнаруживаются различные генетические дефекты.
Они включают в себя анеуплоидии, чаще всего синдром Клайнфельтера, робертсоновские транслокаций, микроделеции Y-хромосомы, мутации рецептора к андрогенам, а также другие мутации (например, муковисцидоз, мутации трансмембранного гена-регулятора проводимости и гена глобулина, связывающего половые гормоны). Таким образом, высокий риск передачи генетических мутаций потомству пациента возникает в случаях необходимости проведения ЭКО с применением ИКСИ.
И все же делать ПГС, если нет «обычных» показаний, или не делать? Есть другие основания для ПГС?
В августе 2016 года было опубликовано исследование, сравнивающее две стратегии:
- Проведение преимплантационного скрининга всем бластоцистам с последующим переносом эмбрионов с известным, нормальным кариотипом.
- Перенос эмбрионов на стадии бластоцисты, но без проведения преимплантационного скрининга.
| Первая группа (с ПГС) | Вторая группа (без ПГС) | |||||||
| Возраст | Количество циклов ЭКО | Количество переносов | Роды | Рождение ребенка /начатый цикл ЭКО | Количество циклов ЭКО | Количество переносов | Роды | |
| ≤34 | 46 | 43 | 35 | 76.1 % | 46.2 % | 65 | 64 | 30 |
| 35–37 | 43 | 41 | 30 | 69.8 % | 48.6 % | 35 | 32 | 17 |
| 38–40 | 47 | 37 | 30 | 63.8 % | 27.8 % | 36 | 35 | 10 |
| 41–42 | 28 | 12 | 8 | 28.6 % | 6.3 % | 16 | 15 | 1 |
| 43+ | 8 | 1 | 1 | 12.5 % | 0.0 % | 8 | 7 | 0 |
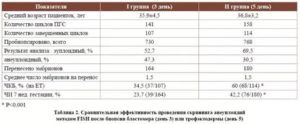
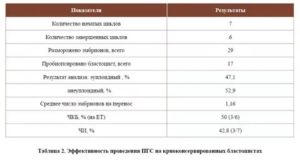
Во всех возрастных группах наблюдается значимая разница по результативности. Но особенно в возрасте 38 и старше. Результативность на начатую программу ЭКО увеличивается в 2 и более раз.
Заключение:
Преимплантационная диагностика переросла в преимплантационный генетический скрининг (ПГС). По мере развития технологии ПГС из групп риска (те у кого выше вероятность эмбрионов с ненормальным кариотипом) начал давать положительный эффект в общей группе пациентов, обращающихся за лечением бесплодия с помощью ЭКО.
Исключение эмбрионов с отклонениями в кариотипе позволяет:
- быстрее добиться беременности,
- избежать выкидышей, связанных с анеуплоидией (бОльшая часть выкидышей),
- исключить рождение детей с хромосомными аномалиями, например, с синдромом Дауна,
- увеличить вероятность рождения ребенка на начатую программу ЭКО.
Чтобы все это получить важны:
- Оценка ВСЕХ хромосом (любой метод),
- Биопсия трофоэктодермы на стадии бластоцисты,
- Высокий профессионализм эмбриолога:
- умение делать бережную и аккуратную биопсию
- если взять слишком мало клеток для биопсии — анализ будет недостоверный, если слишком много – эмбрион может этого и не пережить
- умение выполнять криоконсервацию эмбрионов без потерь
- в таких лабораториях эффективность криопереносов выше, чем свежих
- умение делать бережную и аккуратную биопсию
Источник: http://doctorvladimirov.ru/eko-predimplantatsionnaya-geneticheskaya-diagnostika-pgd-ili-predimplantatsionnyiy-geneticheskiy-skrining-pgs/
Предимплантационный генетический скрининг (ПГС)
В Рижской клинике по лечению бесплодия открыт первый и единственный в Северной Европе Генетический центр, где есть возможность осуществить углублённые генетические обследования.
Современная медицина с каждым днем шире открывает дверь в самые потаенные части человеческого организма, получая больше и больше информации о человеческих генах, их мутациях, приводящих к врожденным патологиям и вероятному бесплодию.
Истинные причины возникновения мужского и женского бесплодия «неясного» происхождения с каждым годом становятся более явными и легко определяемыми, благодаря новейшим разработкам в области репродуктологии и генетики.
Точная и подробная диагностика является залогом успешного лечения, каким бы ни был диагноз.
В Генетическом центре, благодаря инновационным достижениям в области репродуктологии и генетики, у вас будет возможность получить углубленное обследование супружеским парам с бесплодием, невынашиванием беременности, неудачными попытками ЭКО.
Диагностика патологий в клинике
В рамках медико-генетического консультирования врач-генетик собирает анамнез, составляет родословную пары, анализирует существующие риски хромосомной патологии у плода, назначает будущим родителям кариотипирование (генетическое обследование крови).
По итогам врач выдает заключение о необходимости проведения преимплантационной диагностики с указанием метода диагностики, который наиболее актуален в случае конкретной пары.
Генетическое обследование также актуально для пар, которые еще только начинают задумываться о малыше. Пройти медико-генетическое консультирование, включающее всестороннее обследование родителей, рекомендуется еще на этапе планирования беременности, если:
- в Вашей семье или в семьях Ваших родственников были случаи рождения детей с пороками развития, умственной и физической отсталостью, с наследственными или предположительно наследственными заболеваниями, кровное родство, случаи мертворождения
- если Вас интересует прогноз здоровья детей при поздних беременностях (после 35 лет), неблагоприятных воздействиях на плод (болезни матери, лекарственные, физические и химические факторы)
Благодаря новейшим научным достижениям стала возможна преимплантационная генетическая диагностика – исследование клеток эмбриона перед его подсадкой в рамках цикла ВРТ (вспомогательных репродуктивных технологий).
Такую диагностику проводят для того, чтобы будущие родители и врач были уверены, что у эмбриона нет хромосомных аномалий, что во многих случаях и является решением проблемы длительного бесплодия или невынашивания беременности.
Консультации генетика необходимы пациентам перед планированием беременности, если:
- У родителей обнаружены какие-либо генетические заболевания или хромосомные аномалии
- Были неоднократные спонтанные прерывание беременности
- Во время беременности были обнаружены структуральные аномалии плода
- Выявлены изменения в скрининге беременной (отсеивающая диагностика), которые указывают на повышенный риск патологий
Индикации для ПГС (преимплантационный генетический скрининг) методом aCGH (сравнительная геномная гибридизация на микрочипах)
Высок риск образования анеуплоидных (с измененным набором хромосом) эмбрионов при нормальном соматическом кариотипе родителей, если:
- Возраст женщины больше 37 лет
- Возраст женщины больше 35 лет, в случае если развиваются эмбрионы с хорошей морфологией, но беременность не наступает
- Необъяснимая причина бесплодия у молодых пар
- Два или более неудачных циклов ЭКО (при подсадке пяти или более эмбрионов в общем количестве)
- В анамнезе два или более спонтанных абортов (в том числе замерших беременностей)
- В случае плохих показателей качества спермы партнёра (олигоастенотератозооспермия, тяжелая олигозооспермия или азооспермия, плохая морфология сперматозоидов, высокая фрагментация ДНК)
— и при измененном кариотипе родителей высок риск передачи наследственной патологии от родителей будущим детям, если:
- Один или оба родителя являются носителями сбалансированных хромосомальных аберраций (Робертсоновские и реципрокные транслокации)
- Мужской фактор бесплодия, связанный с AZF микроделецией (Y хромосома)
- Один или оба родителя являются носителями мутаций Х хромосомы (например: мышечная дистрофия Дюшена, синдром ломкой Х-хромосомы, Гемофилия и др.)
Преимплантационный генетический скрининг (PGS) методом aCGH
Преимплантационный генетический скрининг основывается на трёх значительных факторах:
- Зачастую для эмбрионов человека характерна анеуплоидия, т. е. изменения в количестве генетического материала (избыток или недостаток) или хромосомные патологии
- В основном анеуплоидия эмбрионов вызывает остановку их развития и как следствие – спонтанный аборт.
- К сожалению, влияние хромосомных патологий на эмбрион незначительно, другими словами – «красивые» эмбрионы могут быть анеуплоидными.
| Возраст пациентки | Генетически нормальные эмбрионы (эуплоиды);% | Эбрионы с генетическими патологиями (анеуплоиды);% |
| 40 | 11 | 89 |
| В среднем | 26 | 74 |
Последствия:
Анеуплоидные эмбрионы могут быть выбраны для трансфера, т. к. визуально выглядят так же хорошо, как и остальные, которые, к сожалению, не были выбраны.
Чаще всего после трансфера анеуплоидных эмбрионов беременность не наступает вообще или возможно прерывание беременности на раннем сроке (до 12 недель развития).
Однако часто подобные хромосомные патологии влияют на развитие плода, в результате чего может родиться ребёнок с синдромом Дауна (трисомия 21-й хромосомы), синдромом Эдвардса (трисомия 18-й хромосомы) или с другим синдромом, характерным для задержки психического или физического развития.
Решение:
Проверять морфологически качественные эмбрионы на генетическом уровне, чтобы перед трансфером выбрать эмбрионы не только с большей вероятностью имплантации в полости матки, но также способные продолжить развиваться.
Данное обследование называют PGS, или преимплантационный скрининг, который можно выполнить методом aCGH. aCGH (сравнительная геномная гибридизация на микрочипах) позволяет протестировать все хромосомы эмбриона одновременно (23 пары) перед переносом эмбриона в полость матки, используя материалы и аппаратуру, созданные, основываясь на новейших научных достижениях.
Таким образом, метод aCGH даёт возможность выбрать лучшие и жизнеспособные эмбрионы, повышая коэффициент имплантации, клинической беременности и долгожданных родов.
Исследование всех 23 пар хромосом методом aCGH сокращает время и усилия для достижения Вашей мечты – стать счастливыми родителями.
Генетический анализ абортного материала
Генетический анализ абортного материала: ответ на вопрос «почему это случилось со мной?»
Клиника в лаборатории репродуктивной генетики проводит генетический анализ абортного материала для пациентов, столкнувшихся с невынашиванием беременности в первом триместре (до 12 недель.
) Анализ проводится методом aCGH (сравнительная геномная гибридизация на микрочипах). С помощью этого метода возможно отличить ткани плода от материнских тканей.
По результатам анализа абортного материала можно с точностью 99% определить и выбрать тактику дальнейшего планирования беременности и избежать повторных негативных результатов.
Генетический анализ абортного материала: что это?
Генетический анализ абортного материала основывается на комплексном анализе всех хромосом.
Данный анализ позволяет определить природу привычного невынашивания беременности и дать чёткий ответ на вопрос, получил ли эмбрион абнормальное количество хромосом (анеуплоидии), послужившее причиной спонтанного аборта.
Результат генетического анализа абортного материала может помочь пациентам найти причину спонтанного аборта и выработать стратегию для успешного зачатия и вынашивания планируемой беременности.
Генетический анализ абортного материала: показания
- Привычное невынашивание беременности (два или более спонтанных абортов)
- Если у пары уже есть ребенок с генетическими отклонениями
- Если у одного из родителей есть изменения в кариотипе
- Если у пары есть подозрения на возможные генетические отклонения
Самые распространенные причины невынашивания беременности в первом триместре (до 12 недель) — спонтанные хромосомные нарушения плода. Основной причиной спонтанного аборта и замершей беременности являются патологии в хромосомном наборе эмбриона.
При оплодотворении яйцеклетки сперматозоидом формирующийся эмбрион может получить абнормальное количество хромосом. Стоит отметить, что риск спонтанного аборта возрастает с репродуктивным возрастом женщины – от 10% в 20-летнем возрасте до 50% в 40-летнем.
Хромосомные нарушения плода при измененном кариотипе у родителей (транслокации)
Изменения в хромосомном наборе родителей также могут послужить причиной невынашивания беременности. Спонтанный аборт может произойти, если один из партнеров является носителем транслокации (хромосомная перестройка, при которой фрагмент одной хромосомы переносится на другую).
Обычно люди, являющиеся носителями транслокаций, не имеют внешних проявлений или симптомов, однако их яйцеклетки или сперматозоиды могут иметь абнормальные хромосомы. Если при оплодотворении яйцеклетки сперматозоидом эмбрион получает неправильное количество генетического материала, чаще всего это приводит к спонтанному аборту – или в худшем случае – к рождению больного ребенка.
Что делать, если Вы столкнулись с невынашиванием беременности?
Если Вы столкнулись с данной проблемой, прежде чем отправиться в стационар для разрешения проблемы замершей беременности, свяжитесь со специалистом по вопросам сбора и транспортировки материала для дальнейшего исследования.
Стоимость услуг центра репродуктивной генетики
- Молекулярное тестирование AZF региона Y-хромосомы — 290 Eur
- Молекулярное тестирование тромбофилии — 150 Eur
- Неинвазивное определение резус-фактора плода — 500 Eur
- Кариотипирование — 150 Eur
- Комплексный анализ: Молекулярное тестирование AZF региона Y-хромосомы и кариотипирование — 410 Eur
Дополнительно о стоимости услуг Центра репродуктивной генетики читайте здесь…
Источник: https://www.evroclinic.com/lechenie-za-rubezhom/lechenie-v-germanii/oblasti-meditsiny/predimplantatsionnyj-geneticheskij-skrining
Эко с преимплантационным генетическим тестированием (пгт)

Эко с преимплантационным генетическим тестированием (пгт)
Преимплантационный генетическое тестирование (ПГТ) — комплекс методик направленных на выявление различных генетических нарушений у эмбрионов. Различают 3 основные разновидности:
ПГТ-А: в недалеком прошлом эту методику называли скринингом (ПГС). Анализ эмбрионов на наличие анеуплоидий — грубых хромосомных нарушений при которых количество хромосом отличается от нормального. Наличие таких нарушений в худшем случае может приводить к рождению детей с генетическими заболеваниями: синдром Дауна, Эдвардса, Патау и прочих.
ПГТ-М: анализ на носительство мутаций в конкретных генах, выхывающих генетические заболевания.
ПГТ-тр: анализ направленный на выявление несбалансированных хромосомных транслокаций у эмюрионов. Это случаи когда в составе одной хромосомы дополнительно оказывается участок другой хромосомы. В итоге получается, что часть генов представлены в организме тремя копиями, что приводит к аномалиям развития.
Показания для проведения ПГС
Для различных методик ПГТ существуют различные показания.
ПГТ-А: строгих показаний к проведению данной методики нет, однако с увеличением возраста женщины генетические аномалии в ооцитах нарастают в геометрической прогрессии.
Эти аномалии могут приводить к замершим беременностям, плохому развитию эмбрионов и к рождению генетически больных детей.
Поэтому рекомендовано задуматься об этом женщинам старше 38 лет, имеющим множественные неудачи в программах ЭКО или с привычным невынашиванием беременности.
ПГТ-М: показанием к проведению данной процедуры является известное носительство моногенного заболевания у одного супруга и особенно у обоих супругов. У пациентов должно быть заключение генетика с указанем того, что за мутация и в каком гене обнаружена. Как правило о наличии такой мутации известно, т.к. есть родственник с моногенным заболеванием.
ПГТ-тр: показанием является наличие сбалансированной хромосомной транслокации у одного из супруга. Выявляется такая транслокация в ходе кариотипирования и никак не проявляется в течении жизни пациента. Поэтому стоит сделать анализ кариотипа, чтобы исключить носительство такой аномалии.
Важно помнить, что, хотя возможен анализ эмбрионов, полученных в результате классического ЭКО, при таком методе оплодотворения повышается вероятность ложноположительного результата — отбраковывания здоровых эмбрионов. Поэтому мы настоятельно рекомендуем проводить оплодотворение с применением ИКСИ даже в отсутствии показаний к применению этой методики.
Как проводится генетическое тестирование
В первую очередь необходимо сделать биопсию — отсечь несколько клеток эмбриона, ДНК которых будет анализироваться. В настоящее время практически во всех случаях проводится биопсия эмбриона 5-х или 6-х суток развития на стадии бластоцисты. Это позволяет отобрать больше материала, тем самым повысив точность анализа, при этом меньше травмируя эмбрион.
Затем материал посылается в генетическую лабораторию на анализ. ПГТ-А делается методом NGS (Next Generation sequencing или секвинирование нового поколения) — самым совершенным на данный момент. ПГТ-М и ПГТ-тр это более специфические процедуры, для которых зачастую требуется проведение продготовительного этапа и обязятельна кровь обоих будущих родителей для изготовления меток.
Безопасна ли процедура для эмбрионов?
Сейчас в мире накоплено достаточно много данных по программам ЭКО и нет оснований утверждать, что процедура снижает шанс на имплантацию эмбриона или несет риски для здоровья ребенка. Однако, нужно понимать, что как и всякую инвазивную процедуру, биопсию эмбриона не стоит проводить в отсутствии показаний.
Что дает ПГТ?
Снижение риска выкидыша: около половины самопроизвольных абортов связаны с хромосомными аномалиями у плода. ПГС позволяет исключить вероятность переноса в матку эмбрионов с отклонениями в числе хромосом и снизить риск выкидыша на ранних сроках беременности.
Повышение вероятности рождения здорового малыша: беременности с хромосомными отклонениями у плода ведут к рождению ребенка с серьезными пороками. С помощью ПГС врачи идентифицируют здоровые эмбрионы, лишенные хромосомных аномалий. Их перенос в матку в программе ЭКО позволяет добиться нормальной беременности и рождения здорового потомства.
Возможность рождения здорового ребенка у пар с известным носительством моногенного заболевания либо с транслокацией.
Преимплантационный генетический скрининг — современная и безопасная репродуктивная технология, доступная пациентам клиники «Новая Жизнь». Благодаря ЭКО с ПГС сотни пар стали счастливыми родителями здоровых малышей!
Стоимость генетической диагностики (ПГТ-А):
Биопсия эмбриона + исследование первого эмбриона методом NGS 60 000 руб
Исследование второго и каждого последующего эмбриона методом NGS 25 000 руб
Источник: https://reprod.ru/collection/eko/product/eko-s-preimplantatsionnym-geneticheskim-skriningom-pgs
Преимплантационный генетический скрининг
в соц. сетях:
21-11-2017
Одной из главных причин неудачных попыток ЭКО, самопроизвольного прерывания последующей беременности и рождения больных детей сегодня считается наличие хромосомных аномалий у плода.
Избежать перечисленных рисков при ЭКО помогает преимплантационный генетический скрининг (ПГС), благодаря которому нарушения обнаруживаются еще на стадии получения эмбрионов, до их переноса в полость матки. Таким образом, для переноса используются только здоровые эмбрионы, благодаря чему многократно увеличиваются шансы на успешную беременность и рождение здорового малыша.
Хромосомные аномалии эмбрионов приводят к невынашиванию беременности
Когда необходимо проведение ПГС
Преимплантационный генетический скрининг не является обязательной процедурой и не входит в стоимость программы ЭКО, но в настоящее время специалисты все больше сходятся во мнении, что ПГС необходим как минимум в половине случаев ЭКО.
На сегодняшний день показаниями к обязательному проведению ПГС являются:
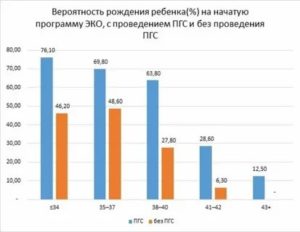
- Возраст женщины старше 35 лет: если у молодых пациенток количество генетически здоровых эмбрионов в среднем составляет почти 80 % от общего количества, то к 40 годам оно снижается до 20 %, а к 44 – 4–5 %.
- Бесплодие неясного генеза.
- Две и более неудачных попытки ЭКО.
- Наличие более двух самопроизвольно прервавшихся, в том числе замерших беременностей.
- Плохие показатели качества спермы мужчины.
Также ПГС оправдан при измененном кариотипе родителей, когда велик риск передачи наследственных патологий. В этом случае может быть показана и преимплантационная генетическая диагностика.
Виды хромосомных нарушений и их последствия
Хромосомные аномалии эмбрионов носят название анеуплоидии. В норме у каждого человека имеется диплоидный или двойной набор хромосом в соматических клетках, который состоит из 22 пар аутосом и 2 половых хромосом. В половых клетках содержится гаплоидный или одинарный набор хромосом, который в момент оплодотворения становится диплоидным.
Отсутствие одной хромосомы в любой хромосомной паре (моносомия) в большинстве случаев вызывает невозможность имплантации эмбриона или же приводит к внутриутробному развитию пороков, не совместимых с жизнью. При нехватке Х-хромосомы развивается синдром Шерешевского-Тернера, который проявляется аномалиями физического развития.
Второй тип анеуплоидии – увеличение хромосомного набора на одну (трисомия), две (тетрасомия) или три (пентасомия) хромосомы. В большинстве случаев патология также несовместима с жизнью, но в ряде случаев приводит к нарушениям у плода.
В частности, вызывает синдром Патау – тяжелые поражения мозга и внутренних органов, синдром Эдвардса – недоразвитие скелетной мускулатуры, деформации стоп и кистей, нарушения развития ЦНС и внутренних органов.
90–95 % случаев возникновения данных состояний приводят к гибели детей на первом году жизни. Наличие дополнительной Х-хромосомы у мальчиков вызывает синдром Кляйнфельтера с наличием разной степени выраженности умственной и физической отсталости, а также нарушениями полового развития.
Одна из наиболее часто встречающихся патологий – синдром Дауна, который проявляется в умственной и физической отсталости.
Преимущества преимплантационного генетического скрининга
Основное преимущество ПГС заключается в возможности отслеживания хромосомных нарушений у эмбриона еще до его переноса в матку, то есть до фактического наступления беременности. Другие методы диагностики, такие как пренатальный скрининг, позволяют обнаружить патологию только по факту, поэтому единственной мерой становится прерывание беременности.
Проведение ПГС в ряде случаев может ускорить наступление беременности методом ЭКО
Использование ПГС в рамках проведения ЭКО повышает шансы на успешную беременность особенно у женщин в возрасте после 40 лет: вероятность успеха в этом случае практически такая же, как у молодой женщины. Главное – получить эмбрион с нормальным кариотипом.
Довольно часто встречаются случаи, когда получить генетически здоровые эмбрионы не удается. Плюс ПГС опять же в том, что увидеть это можно заранее и принять решение о дальнейших действиях: использовании донорских яйцеклеток или же отказ от ЭКО в пользу усыновления.
В настоящее время процедура ПГС хорошо знакома специалистам клиники «ЭКО на Петровке», которые имеют большой опыт в проведении данного исследования. Скрининг проводится путем биопсии, то есть забора нескольких клеток эмбриона на 5–6-е сутки его жизни. Данный метод является малотравматичным и полностью безопасным для эмбриона.
Источник: https://proivf.ru/blog/preimplantatsionnyy-geneticheskiy-skrining/
Преимплантационная генетическая диагностика эмбрионов
- Бесплатная заочная консультация
- Акции клиники
NEXT GENERATION SEQUENCING, NGS
Метод прямого анализа генома эмбриона
Переносздоровых
эмбрионов
Вероятность беременности с ПГД NGS
>74%
Исследование пар хромосом
всех 23
Точность исследования
99,99%
Стоимость ПГДЗаписаться на прием
Критерий назначения – повышенный риск хромосомной или генной патологии. Цель ПГД: идентифицировать эмбрионов без конкретной генетической патологии (генной или хромосомной).
В результате диагностика существенно увеличивает шансы наступления беременности, снижает количество нерезультативных циклов ЭКО и сохраняет здоровье женщины (из-за уменьшения объема принимаемых гормонов).
История NGS в мире и NGC
- 2014 год – рождение первого ребенка после ЭКО c ПГТ методом NGS (Великобритания)
- 2016 год – Санкт-Петербург – рождение первых детей, обследованных на этапе эмбриона методом NGS
- 2017 год – более 300 тестов в год на 1000 эмбрионах. Из них около 300 эмбрионов в высокой вероятности эуплоидии – в стадии криоконсервации.
Методы анализа хромосом на эмбриональном этапе тестирования эмбриона
- FISH – анализ (одна клетка)
- ПЦР (полимеразная цепная реакция)
- arrCGH (геномная гибридизация на микрочипах)
- МПС (массивное параллельное секвенирование ДНК (МПС/NGS) ДНК нескольких клеток)
- Вероятность развития эмбриона (наступления беременности)
- Вероятность нарушений развития эмбриона
- Вероятность тяжелых морфологических нарушений развития плода
- Вероятность обнаружения фенотипических отклонений по УЗИ у плода
- Вероятность нарушений в неонатальный период
- Вероятность ЗПР, когнитивных нарушений полисистемных соматических нарушений
- Качество жизни и здоровья – ребенка и семьи
Применение методов расширенного анализа генома дает комплексный прогноз реализации генетического статуса на всех этапах онтогенеза эмбрион-плод-ребенок и является основой для принятия решения о переносе эмбриона в программах ВРТ.
- Уменьшение числа «безрезультатных переносов».
- Снижение риска спонтанного прерывания беременности.
- Увеличение шансов на беременность у пациентов из групп риска (поздний возраст, носительство транслокаций, многократные неудачные попытки ЭКО).
- Рождение здорового ребенка при риске моногенной патологии
- Снижение риска хромосомной патологии ребенка
- Снижение риска резус-конфликта
- Лечение больного сибса (подбор гистосовместимости)
Целенаправленный анализ отдельных хромосом или генов – моногенные заболевания.Исследование хромосомных аномалий (число и структура хромосом).Комплексный комбинированный анализ — исключение отдельной патологии и случайных нарушений. Например, анализ транслокации и оценка числа хромосом, анализ одного гена и хромосом.
|
Наиболее распространенный метод отбора эмбрионов основан исключительно на их морфологии – не существует корреляции между морфологическим и хромосомным статусом эмбриона.
Риск хромосомных нарушений есть у всех эмбрионов во всех семьях — частота нарушений числа хромосом эмбриона увеличивается с возрастом матери.
Генетический статус эмбриона при ЭКО
ВРТ/ЭКО – c учетом биологического статуса эмбриона не дает:
- Гарантии наступления беременности;
- Гарантии продолжения наступившей беременности;
- Гарантии рождения ребенка;
- Гарантии здорового ребенка.
ЭКО не снижает риски хромосомной патологии и моногенной патологии.
ЭКО как метод лечения бесплодия не дает возможности увеличить вероятность рождения здорового ребенка.
ВРТ/ЭКО проводится в группах популяционного, повышенного и высокого рисков патологии потомства.
По каждому эмбриону был определен:
- Прогноз развития эмбриона (наступления беременности);
- Пренатальный прогноз;
- Постнатальный прогноз;
- Рекомендации по обследованию плода до и после рождения.
трисомия по одной хромосомемоносомия по одной хромосомемножественные анеуплоидиимозаичные формы анеуплоидиймножественные — мозаичные и полные анеуплоидииотклонений не выявлено (рекомендованы к переносу)
- Норма
- Отклонения
- Вероятность наступления беременности
- Вероятность развития беременности по триместрам
- Прогноз для плода
- Необходимость и возможности ПГД
- Вероятность хорион – плацентарных нарушений
- Постнатальный прогноз
Мы сделали анализ на кариотип (кариотипирование) – зачем нам делать ПГД эмбрионов?Классический генетический анализ выявляет измененное число хромосом и крупные структурные нарушения. Его невозможно использовать для клеток эмбрионаПГТ одного эмбриона методом NGS
При условии программы ВРТ в NGC
Биопсия трофектодермы эмбриона
Сделайте первый шаг к счастью!
Отзывы & Что о нас
говорят пациенты
Сеть клиник оснащена самым современным оборудованием
для реализации всех основных направлений ВРТ
Источник: http://old.ngc.clinic/ru/pgs-pgd-ngs/
Пгт и пгс
Специальные структуры в клетках организма, несущие генетическую информацию, называют хромосомами. В норме их должно быть 46 (23 пары). От матери и от отца наследуется по одной копии.
Если эмбрион обладает правильным набором хромосом, его называют эуплоидным. Когда число этих структур изменено, идет речь об анеуплоидии. Такая аномалия становится возможной, если у сперматозоида или ооцита присутствуют избыточные или отсутствуют необходимые хромосомы.
Одним из наиболее распространенных примеров анеуплоидии является синдром Дауна, характеризующийся наличием лишней хромосомы в 21-й паре.
Каковы преимущества преимплантационного генетического тестирования на анеуплоидии (ПГТ-А)?
В настоящее время ПГТ-А является единственным исследованием, способным до переноса эмбриона в полость матки определить, содержит ли он нормальное количество хромосом.
ПГТ-А уменьшает вероятность неудачной имплантации, раннего выкидыша и рождения ребенка с хромосомной патологией, а также повышает шансы на здоровую беременность.
Как выполняется ПГТ-А?
ПГТ-А предполагает исследование нескольких клеток эмбриона, находящегося на стадии бластоцисты (5-6 день развития).
Во избежание ложных результатов тестирования, биопсия бластоцисты осуществляется при ее определенных размерах и хороших морфологических показателях.
Если предполагается проведение ПГТ-А, предпочтителен метод оплодотворения ИКСИ. Это необходимо для того, чтобы избежать попадания ДНК сперматозоидов в образец биопсии.
ПГТ-А может выполняться двумя возможными способами лабораторной диагностики:
- Массивное параллельное секвенирование (NGS)
Массивное параллельное секвенирование нового поколения (next generation sequencing) — это современная технология, которая позволяет проанализировать все 23 пары хромосом, включая половые.
NGS используется прежде всего для определения лишних или отсутствующих копий, небольших дупликаций (удвоение какого-либо участка) или делеций (утрата участка) хромосом. Данный метод обладает самой высокой разрешающей способностью и чувствительностью по определению низкоуровневого мозаицизма.
- Сравнительная геномная гибридизация на чипах (aCGH)
Сравнительная геномная гибридизация (comparative genome hybridization) — это технология, которая также дает возможность осуществить анализ всех 23 пар хромосом.
При выполнении arrayCGH ДНК клеток эмбрионов сравнивается с нормальным контрольным образцом.
Как и NGS, данный метод используется для определения лишних или отсутствующих копий целых хромосом, а также в некоторых случаях позволяет выявить небольшие дупликации или делеции.
Метод сравнительной геномной гибридизации обладает высокой разрешающей способностью и меньшей чувствительностью по выявлению низкоуровневого мозаицизма.
Хотите записаться на прием?
Что такое моногенные заболевания?
Моногенными называют заболевания, обусловленные мутациями в одном из генов. Многие из них являются наследственными, и риск передачи патологии ребенку составляет 25-50%. К наиболее распространенным моногенным заболеваниям относятся муковисцидоз, мышечная дистрофия Дюшенна и серповидноклеточная анемия.
Что такое ПГТ-М на моногенные заболевания?
Исследование позволяет выявить эмбрионы, которые несут моногенное заболевание. ПГТ на моногенные заболевания рекомендуется семейным парам с высоким риском передачи патологии ребенку по результатам медико-генетической консультации. Этот метод позволяет исследовать любой из генов, если известна мутация.
Как проводится ПГТ-М на моногенные заболевания?
Исследование 4-5 клеток эмбриона, полученных в результате биопсии, заметно отличается от генетического тестирования ребенка или взрослого человека.
Из-за ограниченного количества ДНК в клетках для каждой супружеской пары до вступления в программу ЭКО разрабатывается индивидуальная система тестирования.
Для проведения предварительного этапа ПГТ-М требуется образец ДНК от каждого партнера и членов семьи (родителей супругов).
Биопсия эмбрионов, как мы уже говорили выше, проводится на 5-6 день их развития. Полученные клетки анализируют с помощью метода полимеразной цепной реакции (ПЦР).
Оплодотворение осуществляется путем введения сперматозоида непосредственно в цитоплазму ооцита (ИКСИ), чтобы исключить попадание ДНК мужских половых клеток в образец биопсии.
Точность ПГТ-М на моногенные заболевания составляет высокая, но не достигает 100%. Как правило, для повышения вероятности имплантации и наступления беременности дополнительно проводится ПГТ-А на 46 хромосом.
Что такое транслокации / хромосомные перестройки?
Типы хромосомных перестроек:
- транслокации: обмен участками между двумя хромосомами;
- инверсии: участок хромосомы имеет обратную ориентацию;
- делеция: отсутствует участок хромосомы;
- дупликация: есть дополнительный участок хромосомы;
- инсерция:вставка участка одной хромосомы в другую.
При сбалансированной транслокации или инверсии генетическая информация остается верной, но участки хромосомы находятся в другом положении, чем обычно. В таких случаях люди обычно здоровы, но подвержены повышенному риску бесплодия, прерывания беременности и/или рождения ребенка с хромосомной аномалией.
Как проводится ПГТ на хромосомные перестройки?
В качестве материала для этого исследования также используют клетки эмбрионов на стадии бластоцисты. Предоставления образцов родительской крови или проведения предварительного этапа обычно не требуется, но окончательное решение по этому вопросу принимает врач-генетик.
ПГТ на хромосомные перестройки может выполняться методами NGS или aCGH.
Можно ли отличить эмбрионы со сбалансированной транслокацией от тех, у которых ее нет вообще? К сожалению, нет. Основная задача ПГТ — выявление только несбалансированных вариантов перестроек, которые будут сопровождаться комплексом врожденных пороков развития и умственной отсталостью ребенка.
После проведения любого из перечисленных исследований потребуется консультация врача-генетика, который разъяснит полученные результаты и выберет эмбрионы для переноса.
Врачи, выполняющие процедуру
Врач-генетик
Филиал Юго-Западный
9 лет опыта
отзывы
Цены на медицинские услуги
Консультация врача-генетика ПГТ хромосомных аномалий в свежем цикле (стандартная), 1 эмбрион ПГТ хромосомных аномалий (транслокации) в свежем цикле, 1 эмбрион ПГТ моногенных заболеваний (за цикл)
Вернуться к списку
Источник: https://nova-clinic.ru/statyi/pgd-i-pgs/





